Neun B-Vitamine
Zu den essentiellen B-Vitaminen zählen Thiamin (Vitamin B1), Riboflavin (Vitamin B2), Niacin/Niacinamid (Vitamin B3), Pantothensäure (Vitamin B5), Vitamin B6, Folat (Vitamin B11), Vitamin B12, Biotin und Cholin. Die verwandten Nährstoffe Inositol und PABA (para-Aminobenzoesäure) sind offiziell keine B-Vitamine, dennoch aber in vielen Vitamin-B-Komplexen enthalten. B-Vitamine, die in der Nahrung unter anderem in Vollkorngetreide, Obst, Gemüse, Fleisch und Milchprodukten enthalten sind, haben eine breite Wirkungspalette und sind für die normale Funktion, Entwicklung und Erhaltung des Körpers von Bedeutung. Die wasserlöslichen Vitamine werden nur in begrenztem Maße im Körper gespeichert, die tägliche Einnahme ausreichender Mengen dieser Vitamine ist daher wichtig. Ein subklinischer Mangel an B-Vitaminen (insbesondere an Vitamin B6, Folat und Vitamin B12) tritt in westeuropäischen Ländern häufig auf. Gründe dafür sind unter anderem die nicht ideale Ernährungsweise der meisten Westeuropäer und der 10- bis 25-prozentige Verlust der B-Vitamine durch die Lebensmittelverarbeitung und -zubereitung. Darüber hinaus kann durch erbliche Veranlagung, Krankheit oder eine Resorptionsstörung ein erhöhter Bedarf an speziellen B-Vitaminen bestehen. Mit einem guten Multi-Präparat mit B-Vitaminen oder einem Vitamin-B-Komplex wird der normale physiologische Bedarf an B-Vitaminen (reichlich) gedeckt. Zu therapeutischen Zwecken können einzelne B-Vitamine in einer höheren Dosis eingenommen werden. Dabei ist wichtig, zugleich immer auch ein Multipräparat mit B-Vitaminen oder einen Vitamin-B-Komplex einzunehmen, da B-Vitamine in hohem Maße zusammenwirken. Eine positive Entwicklung ist, dass B-Vitamine in Nahrungsergänzungsmitteln immer öfter in ihrer aktiven, coenzymatischen Form (wie sie oft in Nahrungsmitteln enthalten ist) angeboten werden. Dies gilt unter anderem für Vitamin B2 (Riboflavin-5’-phosphat), Vitamin B6 (Pyridoxal-5’-phosphat), Folsäure (5-Methyltetrahydrofolat) und Vitamin B12 (Methyl- und Adenosylcobalamin). Mögliche Probleme bei der Aktivierung von B-Vitaminen werden hierdurch umgangen.
Abbildung 1: B-Vitamine und ihre coenzymatische Form
Zelluläre Energieerzeugung
Alle B-Vitamine spielen in ihrer aktiven, coenzymatischen Form (Abbildung 1) eine lebenswichtige Rolle im zellulären (mitochondrialen) Energiestoffwechsel (Abbildung 2-3). Dabei werden Makronährstoffe aus der Nahrung (Kohlenhydrate, Fette, Proteine) nach Bedarf in Energie (ATP, Adenosintriphosphat) umgesetzt.
Abbildung 2: Die Rolle von B-Vitaminen als Coenzyme bei der Energieerzeugung aus Kohlenhydraten, Fetten und Proteinen
Acetyl-CoA, der Kraftstoff für den Zitronensäurezyklus, entsteht aus Brenztraubensäure/Pyruvat durch oxidative Decarboxylation (Abspaltung von Kohlendioxid nach Oxidation) (Abbildung 3).

Abbildung 3: Die Rolle von B-Vitaminen im Zitronensäurezyklus
Pyruvat fällt durch Aufspaltung von Glucose (Glycolyse) an, wobei zwei Moleküle Pyruvat gebildet werden (Abbildung 3-4). Acetyl-CoA kann auch aus Fettsäuren und bestimmten Aminosäuren gebildet werden. Der Zitronensäurezyklus (Krebszyklus) ist das gemeinsame Eingangstor von Produkten aus der physiologischen Verbrennung von Zuckern, Fettsäuren und Aminosäuren (Abbildung 3-4). Dabei wird Acetyl-CoA in neun Schritten zu 2 Molekülen CO2 oxidiert. Daneben wird Energie erzeugt: Neben einem Molekül Guanosintriphosphat (GTP) entstehen drei Moleküle NADH und ein Molekül FADH2. NADH und FADH2 geben in Cytochromen (speziellen Proteinen mit einer Häm-Verbindung als Co-Faktor) in der inneren Mitochondrialmembran (Abbildung 4) Elektronen an die Atmungskette (Elektronentransportkette) ab, wobei ATP gebildet wird. Dies wird als oxidative Phosphorylierung bezeichnet.

Abbildung 4: Vereinfachtes Schema von Glycolyse (im Cytoplasma), Zitronensäurezyklus (in der mitochondrialen Matrix) und oxidativer Phosphorylierung (in den Cristae der mitochondrialen Innenmembran) mit letztendlicher Bildung von ATP (Energie)
Folsäure, Folat, 5-MTHF
Neben ihrer Rolle im Energiestoffwechsel haben B-Vitamine zahlreiche andere Funktionen. So sind Folat, Vitamin B12, Vitamin B2, Vitamin B6 und Cholin (der Precursor von Betain) für den Folat- und Homocysteinstoffwechsel essentiell (siehe Abbildung 5). Folat (Vitamin B11) in Lebensmitteln umfasst eine Gruppe strukturell verwandter Verbindungen (Pteroylglutamate) mit Vitaminaktivität. Das bekannteste Folat ist ohne Zweifel die Folsäure (Pteroylmonoglutaminsäure), eine gut aufnehmbare und chemisch stabile Verbindung, die in Lebensmitteln kaum enthalten ist und für die Anwendung in Nahrungsergänzungsmitteln und angereicherten Lebensmitteln industriell hergestellt wird. Vitamin B11 steht für die Gruppe der folatwirksamen Verbindungen („Folat“) und nicht nur für die synthetisch hergestellte Folsäure, somit ist es richtiger, für Vitamin B11 die allgemeine Bezeichnung Folat zu verwenden und nicht Folsäure, wie es zumeist geschieht.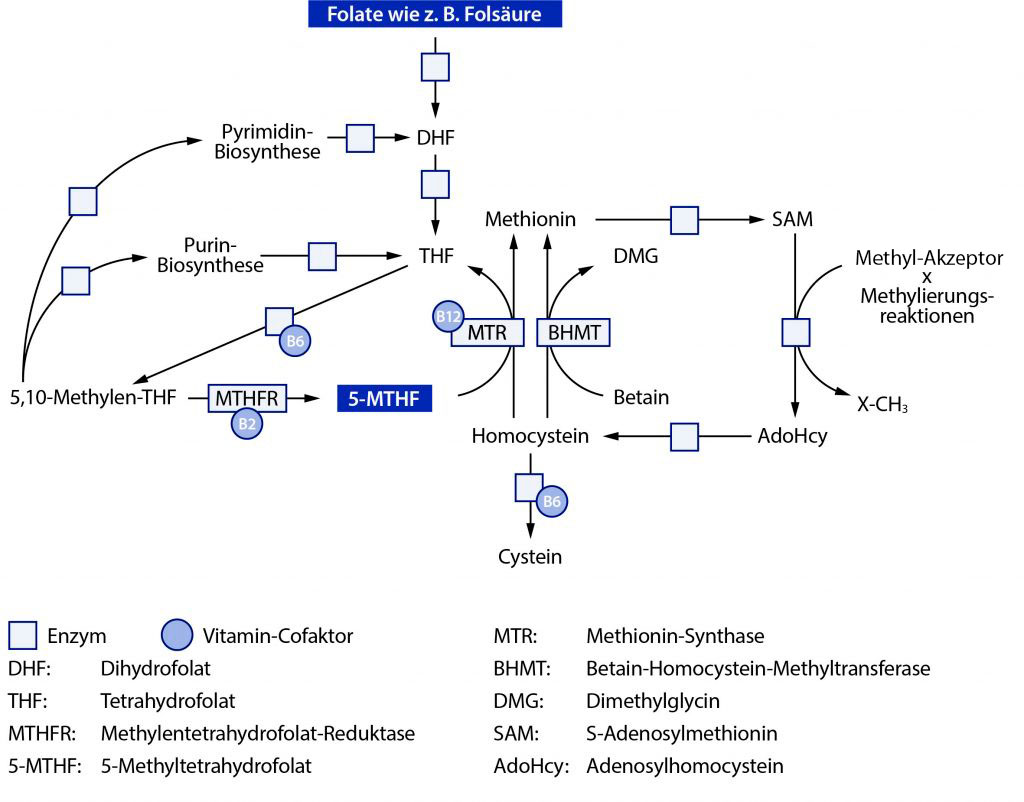
Abbildung 5: Schematische Darstellung des Folat- und Homocysteinstoffwechsels
Folat wird nach der Resorption durch die Enterozyten der Darmwand in Tetrahydrofolat und danach in 5-Methyltetrahydrofolat (5-MTHF), die wichtigste (aktive, coenzymatische) Folat-Form im Körper, umgesetzt. Vitamin B11 zirkuliert in Form von 5-MTHF im Blut und wird so in der Leber gespeichert. Für die Ausnutzung des Folats ist eine gute Magen-Darm-Funktion erforderlich (insbesondere im Duodenum); die Supplementierung mit 5-MTHF hat den Vorteil, dass diese aktive Folat-Form dem Körper garantiert und sofort zur Verfügung steht.
Im Folat- und Homocysteinstoffwechsel fungiert die Coenzym-Form des Folats (5-Methyltetrahydrofolat/5-MTHF) als Methyldonor (Donor von CH3-Gruppen) für die Remethylierung von Homocystein zu Methionin, das dann erneut in den universellen Methyldonor S-Adenosylmethionin umgesetzt werden kann (siehe Abbildung 5). S-Adenosylmethionin (SAM) doniert Methylgruppen (CH3-Gruppen) für die Bildung unter anderem von DNA, RNA, Myelin, Kreatin, Membranphospholipiden, Proteinen und Neurotransmittern.(2) Das Recycling von Homocystein zu Methionin über 5-MTHF und MTR (Methioninsynthase) geschieht im gesamten Körper. In der Leber, den Nieren und Augen kann Homocystein auch über Betain und das Enzym BHMT (Betain-Homocystein-Methyltransferase) recycelt werden. Homocystein kann auch (irreversibel) zu Cystein abgebaut werden, zu diesem Prozess ist Vitamin B6 erforderlich. Cystein ist ein Proteinbaustein und Precursor von Glutathion, einem sehr wirksamen intrazellulären Antioxidans, und zugleich für die Detoxifikation von Xenobiotika von Bedeutung.
Eine andere wichtige Funktion des Folatstoffwechsels besteht in der Lieferung von Methylgruppen für die Synthese von Purinen und Pyrimidinen, Bausteinen der Nukleinsäuren DNA und RNA (siehe den linken Teil von Abbildung 5). Weiterhin ist Folat an der Synthese von Hämoglobin, der (fetalen) Entwicklung des zentralen Nervensystems und der Umsetzung der Aminosäure Serin zu Glycin beteiligt. Folat in Lebensmitteln wie Gemüsen (vor allem grünen Blattgemüsen), Obst, Bohnen, Innereinen und Fleisch ist instabil und empfindlich gegenüber Licht, Sauerstoff, Lagerung und hohen Temperaturen, wodurch ein großer Teil des Folats verloren geht. Deshalb ist es selbst bei einer gesunden Ernährungsweise fast unmöglich, ausreichend Folat aus der Nahrung zu gewinnen. Ein reduzierter Folatstatus/Folatmangel ist daher einer der häufigsten Nährstoffmängel.
Die Aminosäure Homocystein ist ein Stoffwechsel-Zwischenprodukt und für den Körper schädlich. Ein Anstieg des Homocysteinspiegels kann die Folge eines Mangels an Folat, Vitamin B12, Vitamin B6, Vitamin B2 oder Betain sein oder von Genmutationen der Enzyme MTHFR (Methylentetrahydrofolat-Reduktase) oder MTR, wodurch diese nicht richtig funktionieren. Bei einem Folatmangel oder einer MTR-Dysfunktion (durch ein verändertes Gen, einen Vitamin-B12-Mangel oder einen gestörten Vitamin-B12-Stoffwechsel) stockt der Folatzyklus und die Synthese der Purine und Pyrimidine gerät in Gefahr. Ein Mangel an Purinen und Pyrimidinen wirkt sich vor allem auf sich schnell teilende Zellen wie die Zellen des Knochenmarks aus, dies hat Blutbildstörungen (megaloblastäre Anämie*, Panzytopenie*) zur Folge. Eine reduzierte MTHFR-Aktivität beeinträchtigt nicht die Purin- und Pyrimidin-Synthese und führt nicht zu Veränderungen des Blutbilds.
MTHFR-Polymorphismus
Das von Vitamin B2 abhängige Enzym 5,10-Methylentetrahydrofolat-Reduktase (MTHFR) ist für die Synthese von 5-Methyltetrahydrofolat (5-MTHF, die aktive Folat-Form) verantwortlich und innerhalb des Homocystein-Stoffwechsels geschwindigkeitsbestimmend. Eine häufig vorkommende Mutation des MTHFR-Gens, bei der auf dem Nukleotid* 677 Cytosin* durch Thymin* ersetzt ist (677C?T- oder C677T-Polymorphismus*), führt zur verminderten Aktivität des Enzyms MTHFR. In der europäischen Bevölkerung haben hinsichtlich dieses Polymorphismus 45% das normale Gen (CC-Genotyp, Wild-type*), sind ca. 12% homozygot* (TT-Genotyp*) und 43% heterozygot* (CT-Genotyp*).(3,4) Beim TT-Genotyp ist die MTHFR-Aktivität (in vitro) um 75 % geringer und beim CT-Genotyp um 40% geringer als beim CC-Genotyp. Dies führt zum Anstieg des Homocysteinspiegels und zur Abnahme der Methylierungsprozesse, da die Produktion von 5-MTHF insbesondere bei einer geringen Folateinnahme abnimmt.(3) In der Leber, den Nieren und den Augen wird Homocystein noch über Betain und das Enzym BHMT (Betain-Homocystein-Methyltransferase) recycelt, aber dieser Prozess gerät unter großen Druck.
Eine verminderte MTHFR-Aktivität (und andere Ursachen für eine Hyperhomocysteinämie und die Abnahme von Methylierungsprozessen) wurde mit einer Reihe von Erkrankungen assoziiert, darunter Herz-Kreislauferkrankungen (unter anderem Hypertonie, Präeklampsie, Venenthrombose, Atherosklerose, Schlaganfall, Bauchaorten-Aneurysma), angeborene Fehlbildungen (Spina bifida, congenitaler Herzfehler, LKGS-Spalten), Unfruchtbarkeit, Schwangerschaftskomplikationen (Fehlgeburten, Frühgeburt, niedriges Geburtsgewicht), Diabetes (-komplikationen), Krebs (unter anderem Brust-, Gebärmutterhals- und Schilddrüsenkrebs, chronische myeloische Leukämie), (periphere) Neuropathie, verschiedene neurodegenerative und psychiatrische Erkrankungen (darunter Schizophrenie, Depression, Autismus, Morbus Alzheimer, Morbus Parkinson), Down-Syndrom, Vitiligo, Osteoporose, Nierenversagen und rezidivierende aphthöse Stomatitis (Mundaphthen).(2,5-21) Dies impliziert, dass eine (präventive) Verbesserung des Folatstatus mit 5-MTHF großen Gewinn für die Gesundheit bringen kann.
Supplementierung mit 5-MTHF
Folat (darunter Folsäure) wird nach der Einnahme zu THF (Tetrahydrofolat) reduziert und danach von MTHFR zu 5-MTHF umgesetzt, wobei dieser Prozess langsam und ineffizient ist und noch viel schlechter abläuft, wenn die MTHFR-Aktivität vermindert ist.(3) In Humanstudien wurde nachgewiesen, dass hinsichtlich der Verbesserung des Vitamin-B11-Status und der Absenkung des Homocysteinspiegels die Supplementierung mit 5-MTHF effektiver ist als die mit Folsäure, und dies gilt sowohl für den TT-Genotyp als auch für den CT- und den (normalen) CC-Genotyp von MTHFR.(3,22) Auch angesichts des großen Prozentanteils von Menschen mit C677T-Polymorphismus ist anzuraten, bei einer Folat-Supplementierung immer 5-MTHF und nicht Folsäure zu wählen.
Die Bindung von 5-MTHF als Glucosaminsalz macht es möglich, die biologisch aktive Form stabil zu halten, und sorgt für optimale Resorbierbarkeit. Darüber hinaus kann die Verbindung im Gegensatz zur „normalen“ Folsäure die Blut-Hirn-Schranke passieren. Auch gibt es Hinweise darauf, dass das als Glucosaminsalz gebundene 5-MTHF eine höhere Wasserlöslichkeit, Stabilität und biologische Verfügbarkeit hat als das als Calciumsalz gebundene 5-MTHF (Abbildung 6).

Abbildung 6: Unterschiedliche biologische Verfügbarkeiten des 5-MTHF-Glucosaminsalzes, des 5-MTHF-Calciumsalzes und von Folsäure(53)
Die Supplementierung mit einer hohen Dosis Folsäure kann vor allem bei Menschen mit MTHFR-Polymorphismus zur Akkumulation nicht-metabolisierter Folsäure im Blut führen. Dies ist möglicherweise gesundheitsschädlich (dass Folsäure Krebs fördern würde, ist in einer kürzlichen Metaanalyse übrigens widerlegt worden) und kann einen Vitamin-B12-Mangel maskieren.(23-26) Wenn mit 5-MTHF supplementiert wird, treten diese Probleme wahrscheinlich nicht auf.(23) Vorzugsweise wird 5-MTHF zusammen mit anderen B-Vitaminen eingenommen, in jedem Fall mit Vitamin B12, Vitamin B6 und Vitamin B2.(25) Folat selbst ist wenig toxisch; ebenso wie bei anderen B-Vitaminen wird ein Zuviel mit dem Urin ausgeschieden. Jedoch wurde der UL (Tolerable Upper Intake Level) für (synthetische) Folsäure auf 1000 µg/Tag festgelegt, da eine höhere Dosis einen Vitamin-B12-Mangel maskieren kann. Die Supplementierung mit 5-MTHF-Glucosamin in einer höheren Dosis als 1000 µg/Tag ist in dieser Hinsicht wahrscheinlich unbedenklich (doch gilt auch für 5-MTHF ein UL von 1000 µg/Tag), insbesondere wenn gleichzeitig ausreichend Vitamin B12 zugeführt wird.(27,28) Die empfohlene Tagesdosis (RDA) für Folat beträgt 300 µg/Tag, in der Perikonzeptionsphase 700 µg/Tag, während der Schwangerschaft 400 µg/Tag und in der Stillzeit 400 µg/Tag.(27,28)
Vitamin B12
Vitamin B12 ist ein essentieller Nährstoff, der unter anderem bei der DNA-Synthese, zellulären Reparaturprozessen, der Blutbildung und Hirnfunktion eine bedeutende Rolle spielt. Ein abgesenkter Vitamin-B12-Status kann ein sehr breites Spektrum von Gesundheitsproblemen verursachen. Vitamin B12 ist ein unabdingbarer Co-Faktor bei zwei wichtigen enzymatischen Reaktionen:• In Form von Methylcobalamin (im Cytoplasma) ist Vitamin B12 Co-Faktor bei der (Re-) Methylierung von Homocystein zu Methionin durch das Enzym Methionin-Synthase (MTR, siehe Abb. 5). Dabei wird 5-Methyltetrahydrofolat zu Tetrahydrofolat umgesetzt, wichtig für die RNA- und DNA-Synthese.
• In Form von Adenosylcobalamin (in Mitochondrien) ist Vitamin B12 an der Umsetzung von Methylmalonyl-CoA zu Succinyl-CoA durch das Enzym Methylmalonyl-CoA-Mutase beteiligt (siehe Abb. 3, AdoB12), wichtig unter anderem für den Fettsäure-, Cholesterol- und Proteinstoffwechsel, den Energiestoffwechsel und die Hämoglobinsynthese.
Das wasserlösliche Vitamin B12 besteht aus einer Reihe von Cobalaminen, komplex aufgebauten Molekülen mit einem Kobaltatom im Zentrum. Vitamin B12 kommt in verschiedenen Formen vor, je nachdem welche Restgruppe an das zentrale Kobaltatom gebunden ist: Methyl-, Adenosyl-, Hydroxy- und Cyanocobalamin (der Term Cobalamin verweist immer auf eine dieser Formen). Cyanocobalamin ist eine synthetische Form, die viel in Nahrungsergänzungsmitteln und angereicherten Lebensmitteln eingesetzt wird. Der Vorteil eines Nahrungsergänzungsmittels mit den biologisch aktiven (coenzymatischen) Formen Methyl- und Adenosylcobalamin besteht darin, dass das Vitamin B12 dem Körper sofort zur Verfügung steht. Untersuchungen legen nahe, dass sich der Cobalamin-Status nach Einnahme von Methyl- und Adenosylcobalamin stärker verbessert als nach Einnahme von Cyanocobalamin: Es wird mehr Cobalamin in der Leber gespeichert und weniger Cobalamin mit dem Urin aus dem Körper ausgeschieden (längere Halbwertszeit).(47) Außerdem kann Methylcobalamin im Körper sofort als Methyldonor verwendet werden. Es gibt Hinweise darauf, dass die Supplementierung mit Methyl- und/oder Adenosylcobalamin bessere klinische Ergebnisse liefert als die Supplementierung mit Cyano- und/oder Hydroxycobalamin.
Vitamin B12 ist ein sehr sicheres Ergänzungsmittel (auch während der Schwangerschaft und Stillzeit), und es hat auch in sehr hohen Dosierungen (von Tausenden Mikrogramm pro Tag) keine Nebenwirkungen. Eine tolerierbare Höchstaufnahmemenge wurde daher nicht festgelegt. Die Menge Vitamin B12 in einem guten Multi-Präparat und Vitamin-B-Komplex deckt den normalen Vitamin-B12-Bedarf reichlich. Der Vitamin-B12-Bedarf ist wahrscheinlich größer als die gegenwärtig empfohlene Tagesdosis (RDA) von 2,5 µg/Tag (3,2 µg/Tag während der Schwangerschaft und 3,8 µg/Tag in der Stillzeit) und kann bis über 20 µg/Tag betragen.(30) Mit zunehmendem Alter wird Vitamin B12 oft weniger gut aus der Nahrung aufgenommen (gut jedoch aus einem Nahrungsergänzungsmittel). Personen mit vegetarischer Ernährung nehmen in der Regel weniger Vitamin B12 zu sich. In diesen und anderen Situationen, in denen die Aufnahme von Vitamin B12 zu wünschen lässt, garantiert ein Multi oder Vitamin-B-Komplex, dass Vitamin B12 in ausreichender Menge zugeführt wird. Schätzungsweise haben etwa 5 bis 10% der westeuropäischen Bevölkerung einen Vitamin-B12-Mangel, in der Gruppe der Älteren kann dieser Prozentanteil auf 20 bis 30% ansteigen. Bei einer Vitamin-B12-Malabsorption und bei spezifischen Indikationen für eine Vitamin-B12-Supplementierung ist ein gesondertes, hoch dosiertes Vitamin-B12-Ergänzungsmittel erforderlich.
Vitamin B6
Vitamin B6 ist an über 100 Enzymreaktionen im Körper beteiligt, die vor allem mit der Energieproduktion und dem Fett- und Proteinstoffwechsel in Verbindung stehen. Vitamin B6 trägt zur Absenkung des Homocystein- und Cholesterolspiegels bei und hat dadurch eine positive Wirkung auf Herz und Blutgefäße und den Hirnstoffwechsel. Auch an der Bildung von Hämoglobin, Myoglobin*, Nukleinsäuren (DNA, RNA) und Neurotransmittern wie z. B Serotonin und GABA ist Vitamin B6 beteiligt. Weiterhin ist Vitamin B6 für die einwandfreie Funktion des Immunsystems und des endokrinen Systems wichtig. Ein Vitamin-B6-Mangel erhöht den Homocysteinspiegel und kann Rhagaden in Lippen und Mundwinkeln (Cheilitis), eine entzündete Zunge, seborrhoische Ekzeme*, periphere Neuropathie, Mattigkeit, Depressionen, eine Verschlechterung der kognitiven Fähigkeiten, verminderte Widerstandskraft, Migräne und Blutarmut verursachen. Ein subklinischer Vitamin-B6-Mangel ist häufig, insbesondere bei Senioren, Alkoholikern, Schwangeren und Personen mit erhöhtem Vitamin-B6-Bedarf (bedingt durch Krankheit, Arzneimittelgebrauch oder Stress).(31) Um eine gute Vitamin-B6-Zufuhr zu gewährleisten, wird die Einnahme eines Multi-Präparats oder Vitamin-B-Komplexes mit Vitamin B6 (vorzugsweise in Form von Pyridoxal-5’-phosphat) empfohlen. Vitamin B6 besteht eigentlich aus 6 verwandten Verbindungen, von denen Pyridoxal-5’-phosphat (P5P) die wichtigste ist. Die Supplementierung mit Vitamin B6 in Form von P5P hat den Vorteil, dass das Vitamin vom Körper (speziell in der Leber) nicht mehr in diese biologisch aktive Form umgesetzt werden muss, ein Prozess, der nicht bei allen Menschen gleich effizient verläuft. Außerdem kann man wegen der besseren Aufnahme und Wirksamkeit mit einer geringeren Dosierung auskommen.(31,32)Vitamin B6 – Akkumulation
Viele Menschen machen sich Sorgen über mögliche Nebenwirkungen (insbesondere Neurotoxizität) einer Vitamin-B6-Supplementierung. Die tolerierbare Höchstaufnahmemenge (UL, tolerable upper intake level) für Vitamin B6 wurde für Erwachsene in Europa auf 25 mg/Tag und in den Vereinigten Staaten auf 100 mg/Tag festgelegt.(45,46) Der Grund ist, dass Vitamin B6 (insbesondere Pyridoxin) in vereinzelten Fällen und aus unklaren Gründen schon bei einer (sehr) geringen Dosis Beschwerden einer sensorischen Polyneuropathie (Kribbeln in Händen und Füßen, Taubheitsgefühl, verminderter Tastsinn, unsicheres Laufen, Schmerzen in den Gliedmaßen) verursacht hat.(33) In der Mehrheit der Fälle einer sensorischen Polyneuropathie handelte es sich allerdings um eine langfristige Einnahme von mindestens 500 mg Vitamin B6 pro Tag (8 mg/kg/Tag). Der LOAEL (lowest observed adverse effect level) wurde daher auf 500 mg/Tag festgelegt. Die maximale Dosis, die von den meisten Menschen ohne das Auftreten von Nebenwirkungen vertragen wird (NOAL, no observed adverse effect level), beträgt 200 mg/Tag. Die Supplementierung mit Vitamin-B6-Dosierungen bis zu 200 mg/Tag sollte daher nur selten Probleme bereiten. In der Praxis werden Beschwerden jedoch manchmal schon bei Dosierungen wahrgenommen, die niedriger sind als der NAOL. Es ist daher weiterhin wichtig, auf mögliche Symptome der sensorischen Neuropathie zu achten, die nach der Einnahme von Vitamin B6 entstanden sind (Anmerkung: Ein Vitamin-B6-Mangel kann ebenfalls Neuropathie verursachen). Die Einnahme von Vitamin B6 sollte dann sofort beendet werden, und die Beschwerden verschwinden danach nahezu immer innerhalb weniger Monate. Weshalb manche Menschen nach Einnahme einer relativ geringen Dosis Vitamin B6 neuropathische Beschwerden entwickeln, ist nicht ganz klar (auch fehlt eine Korrelation zwischen neuropathischen Beschwerden und dem Vitamin-B6-Spiegel im Blut). Als Ursache wird eine unzureichende Umsetzung von Pyridoxin zu Pyridoxal-5’-phosphat vermutet (zum Beispiel aufgrund einer gestörten Leber- oder Nierenfunktion oder eines Mangels an dem Enzym alkalische Phosphatase), wodurch der Spiegel des freien Pyridoxins zu stark ansteigt (NB: In Blutuntersuchungen wird der P5P-Spiegel gemessen, und es ist normal, dass dieser bei einer Vitamin-B6-Supplementierung ansteigt).(48-51) In Tierstudien wurde festgestellt, dass sehr hohe Pyridoxin-Dosen für das Nervengewebe schädlich sind (Neurotoxizität), während dies bei anderen Formen von Vitamin B6 wie Pyridoxal-5’-phosphat nicht der Fall ist.(52) Dies ist ein weiterer Grund, sich für einen Multi oder Vitamin-B-Komplex mit Pyridoxal-5’-phosphat zu entscheiden.(31,32) Aber auch hier gibt es in Praxis Erfahrungen, dass manche Menschen einfach besser auf Pyridoxin ansprechen als auf P5P und dass auch P5P sporadisch Beschwerden hervorrufen kann. Eine individuelle Vorgehensweise und Wachsamkeit beim therapeutischen Verschreiben höherer B6-Dosierungen bleiben daher wichtig.
Vitamin B1
Vitamin B1 (Thiamin) ist als Coenzym (Thiaminpyrophosphat, TPP) für die Energieerzeugung aus Kohlenhydraten unverzichtbar und unterstützt damit Organe, die für ihre Energieerzeugung weitgehend von Kohlenhydraten abhängig sind, also z. B. Muskeln, Herz und das zentrale und periphere Nervensystem. TPP ist essentiell für die Umsetzung von Pyruvat zu Acetyl-CoA (siehe Abbildung 3). Bei einer Unterversorgung mit Vitamin B1 können Kohlenhydrate nicht richtig als Energiequelle genutzt werden. Darüber hinaus trägt Vitamin B1 dazu bei, den oxidativen Stress auf Zellebene zu senken, und spielt im Fettstoffwechsel und bei der Synthese von Hormonen, Neurotransmittern, DNA und RNA, Proteinen und Enzymen eine Rolle. In Nervenzellen fördert TPP eine gute Reizleitung. Zudem unterstützt Vitamin B1 die exokrinen und endokrinen Funktionen der Bauchspeicheldrüse; ein Vitamin-B1-Mangel kann dazu führen, dass weniger Verdauungsenzyme gebildet werden und die Insulinsynthese und -sekretion abnimmt.(34) Ein niedriger Thiaminstatus potenziert die (Neuro-) Toxizität von Blei, während eine Thiamin-Supplementierung die Bleikonzentration in Blei, Nieren und Knochen absenkt (das Blei wird dabei an den Pyrimidinring des Thiamins gebunden).(35,36) Ein reduzierter Thiaminstatus führt zu unspezifische Beschwerden wie Ermüdung, Reizbarkeit, Konzentrations- und Gedächtnisproblemen, Appetitlosigkeit, Gewichtsverlust, Schlafstörungen, Niedergeschlagenheit, Muskelschwäche und Bauchschmerzen. Zu einem abgesenkten Thiaminstatus können unter anderem eine Thiamin-Malabsorption (bei Alkoholkrankheit, Leberzirrhose, Magen-Darm-Erkrankungen) führen, eine zu geringe Zufuhr von Thiamin mit der Nahrung (bei Magersucht, Erbrechen, Alkoholkrankheit, Senioren) oder ein erhöhter Thiaminbedarf (unter anderem bei Stress, einer hohen Kohlenhydratzufuhr, schwerer körperlicher Arbeit, Diabetes mellitus, Hyperthyreose, Infektionen, Lebererkrankungen, Arzneimittel-Einnahme). In den westlichen Ländern ist Alkoholismus die Hauptursache für einen schweren Thiaminmangel, der zum Wernicke-Korsakow-Syndrom (Verlust des Kurzzeitgedächtnisses, Demenz, Delirium) führt. Die klassische Thiaminmangelkrankheit Beriberi (mit neurologischen und kardiovaskulären Symptomen) ist in Westeuropa selten.Die Thiamin-Supplementierung ist sehr sicher, eine Obergrenze (UL, upper limit) wurde nicht festgelegt. Die empfohlene Tagesdosis RDA beträgt für Erwachsene 1,1 mg/Tag (in der Schwangerschaft 1,4 mg/Tag; in der Stillzeit 1,7 mg/Tag). Eine übliche therapeutische Dosierung beläuft sich auf 100 bis 300 mg Thiamin pro Tag.
Vitamin B2
Riboflavin ist Bestandteil der Coenzyme Flavinmononukleotid (FMN; Synonym: Riboflavin-5’-phosphat) und Flavin-Adenin-Dinukleotid (FAD), die unter anderem an Redoxreaktionen im Energiestoffwechsel beteiligt sind. Die Flavin-Coenzyme sind auch wichtig für den Stoffwechsel von Steroidhormonen, den Fettstoffwechsel und die Aktivität verschiedener Enzyme (darunter Glutathion-Reduktase* und Cytochrom P450*). MTHFR ist ebenso ein von Vitamin B2 abhängiges Enzym. In einer klinischen Studie führte die Supplementierung mit Riboflavin (1,6 mg/Tag) bei Personen mit Hypertonie und dem homozygoten Genotyp (TT-Genotyp) für MTHFR (C677T) zu einer signifikanten Absenkung des Blutdrucks, vermutlich teilweise aufgrund einer Verbesserung der MTHFR-Aktivität.(29) Darüber hinaus ist Vitamin B2 (zusammen mit Vitamin B6) als Coenzym an der Umsetzung der Aminosäure Tryptophan zu Niacin (Vitamin B3) und der Synthese der aktiven Form von Vitamin B6 (Pyridoxal-5’-phosphat) aus Pyridoxin beteiligt. Vitamin B2 ist wichtig für den Eisenstoffwechsel. Ein Riboflavinmangel führt unter anderem zur Abnahme der antioxidativen Kapazität (durch Absenkung der Aktivität der Glutathion-Reduktase und der eigenen antioxidativen Wirkung), zur Erhöhung des Homocysteinspiegels und zu Blutarmut. Andere (spezifische) Symptome eines Riboflavinmangels: entzündete Mundwinkel, trockene Lippen mit Rhagaden (Cheilitis), geschwollene und rote Schleimhäute von Mund und Rachen, entzündete Zunge (Glossitis), seborrhoisches Ekzem (vor allem um die Nase und zwischen Nase und Lippen), Augenbeschwerden (Lichtempfindlichkeit, Brennen, Jucken, Tränen). Ein erhöhtes Risiko für einen Riboflavinmangel besteht u. a. bei Diabetes mellitus, Herzerkrankungen, Krebs, Malabsorption, Nierendialyse und Arzneimittelgebrauch (darunter Antibabypille, Antipsychotika, trizyklische Antidepressiva).
Abbildung 7: Strukturformeln von Riboflavin und der aktiven Coenzym-Form Riboflavin-5’-phosphat (FMN)
Die Umsetzung von Riboflavin zu FMN und FAD hängt vom Schilddrüsenhormon ab. Bei Personen mit (milder) Hypothyreose wurde festgestellt, dass der Homocysteinspiegel durch Reduzierung der Synthese von FMN (Riboflavin-5’-phosphat) und FAD ansteigt. Die Umsetzung von Riboflavin in die Coenzym-Formen kann auch bei anderen Erkrankungen vermindert sein. Auch deshalb ist die Supplementierung mit Riboflavin-5’-phosphat (der natürlichen aktiven, coenzymatischen Form von Vitamin B2 in der Nahrung) einer Supplementierung mit Riboflavin vorzuziehen. Die empfohlene Tagesdosis RDA beträgt für erwachsene Frauen 1,1 mg/Tag (in der Schwangerschaft 1,4 mg/Tag; in der Stillzeit 1,7 mg/Tag) und für erwachsene Männer 1,5 mg/Tag. Es sind keine toxischen Wirkungen oder Nebenwirkungen von Riboflavin bekannt. Eine tolerierbare Höchstaufnahmemenge (UL, upper limit) wurde nicht festgelegt.
Die Supplementierung mit Riboflavin kann zu einer (harmlosen) hellgelben Färbung des Urins führen.
Vitamin B3
Es gibt zwei Formen von Vitamin B3, nämlich Niacin (Nikotinsäure) und Niacinamid (das Amid der Nikotinsäure). Vitamin B3 nimmt bei der Bildung von zwei der wichtigsten Coenzyme im Körper eine Schlüsselstellung ein: NAD (Nicotinamid-Adenin-Dinukleotid, Coenzym I) und NADP (Nicotinamid-Adenin-Dinukleotid-Phosphat, Coenzym II), die an über zweihundert biochemischen Reaktionen beteiligt sind.
Abbildung 8: Vitamin B3 als Niacin und Niacinamid
Vitamin B3 kann im Körper in begrenztem Maße aus Tryptophan gebildet werden. Vitamin B3 ist für den Kohlenhydrat , Fett- und Proteinstoffwechsel und eine große Anzahl Hormone, Neurotransmitter und Enzyme bedeutsam sowie auch für die Energieproduktion in den Zellen. In physiologischen Mengen sind Niacin und Niacinamid austauschbar. Für Multi-Präparate und Vitamin-B-Komplexe wählt man oft Niacinamid, weil Niacin einen unangenehmen „Flush“ verursachen kann (ähnlich einer menopausalen Hitzewallung, jedoch ohne Schwitzen). Die typische Vitamin-B3-Mangelkrankheit ist Pellagra, gekennzeichnet durch die drei D’s: Dermatitis, Durchfall und Demenz. Der durchschnittliche Niacinbedarf (AR, average requirement) für Erwachsene beträgt 5,5 mg NE (Niacin-Equivalente) pro 1000 kcal pro Tag; die empfohlene Tagesmenge (RDA) beträgt 16 mg/Tag.(37) Die tolerierbare Höchstaufnahmemenge (UL, upper limit) für Niacinamid beträgt 900 mg/Tag und für Niacin 10 mg/Tag (oberhalb dieser Mengen kann ein harmloser, aber manchmal unangenehmer Flush auftreten).
Vitamin B5
Vitamin B5 (Pantothensäure) ist in Form von Coenzym A (CoA) und sogenannten Acyl Carrier Proteins (ACP)* für das Wachstum, die Fortpflanzung und die normalen physiologischen Funktionen essentiell. Vitamin B5 ist an der Energieproduktion, dem Kohlenhydrat-, Protein- und Fettstoffwechsel, der Phase-II-Detoxifikation, dem Stoffwechsel anderer B-Vitamine und der Synthese von Neurotransmittern, Steroidhormonen, Porphyrinen*, Prostaglandinen, Phospholipiden und Hämoglobin beteiligt.(38) Zudem ist Vitamin B5 wichtig für die Nebennierenfunktion und die Stressresistenz. Pantothensäure ist in vielen Nahrungsmitteln enthalten (das griechische „pantos“ bedeutet „überall“), jedoch kann der Vitamin-B5-Gehalt der Nahrung durch die industrielle Verarbeitung, das Kochen, Einfrieren und Konservieren in Dosen stark abnehmen. Dennoch ist ein ausgeprägter Pantothen-Mangel in Westeuropa selten. Ein subklinischer Pantothen-Mangel ist unter anderem aufgrund von schlechten Essgewohnheiten, hohem Alkoholkonsum und Stress möglich. Die adäquate Einnahme (Adequate Intake, AI) für Vitamin B5 beträgt 5 mg/Tag. Die Toxizität von Pantothensäure ist äußerst gering, eine tolerierbare Höchstaufnahmemenge (UL, upper limit) wurde daher nicht festgelegt.
Biotin
Biotin, ein kürzlich entdecktes wasserlösliches B-Vitamin, ist Coenzym für fünf Carboxylasen, Enzyme, die unter anderem in der Glucose- und Fettverbrennung, Fettsäuresynthese, Gluconeogenese und im Aminosäure-Stoffwechsel eine Rolle spielen. Darüber hinaus wird Biotin an Histone gebunden, wichtige strukturgebende Proteine in Chromosomen, die sicherstellen, dass die DNA kompakt gefaltet wird, und auf diese Weise zur Stabilität des Genoms beitragen (Abbildung 9).
Abbildung 9: Die DNA in Chromosomen ist um Nukleosomen (aufgebaut aus mehreren Histonen) herumgewunden
Biotin wirkt eng mit Folat, Pantothensäure, Vitamin B12 u.a.m. zusammen. Biotin ist wichtig für gesunde Haut, gesundes Haar und gesunde Nägel und hemmt möglichen Haarausfall und das Ergrauen der Haare. Ein geringfügiger Biotinmangel während der Schwangerschaft erhöht wahrscheinlich das Risiko für angeborene Fehlbildungen.(39) Erhöhter Biotinbedarf besteht bei einer Nierendialyse, hohem Alkohol- oder Kaffeekonsum, Magenerkrankungen, entzündlichen Darmerkrankungen, in der Schwangerschaft/Stillzeit, durch Rauchen, Verzehr von rohen Eiern und die Einnahme von Arzneimitteln (Sulfonamid-Antibiotika, Antikonvulsiva, Isotretinoin und Antibabypille). Mögliche Symptome eines Biotinmangels sind dünner werdendes Haar, Alopezie, brüchige Nägel, Konjunktivitis, Hautinfektionen, trockene Haut, Hautausschlag rund um Augen, Nase und Mund und eine verringerte Widerstandskraft.(40) Es ist nicht genau bekannt, wie hoch der Biotinbedarf wirklich ist. Die adäquate Einnahme (Adequate Intake, AI) für Biotin wird bei Erwachsenen auf 30-100 µg/Tag geschätzt. Es ist möglich, dass für einen guten Schutz der DNA eine höhere Zufuhr erforderlich ist.(41) Biotin ist ein sehr sicherer Nährstoff, selbst in sehr hohen therapeutischen Dosierungen (bis zu 200 mg/Tag bei erblich bedingtem Biotinidase-Mangel*).
Cholin
Cholin wurde 1998 als essentieller Nährstoff für den Menschen anerkannt.(42) Cholin ist (nach der Umsetzung zu Betain) als Methyldonor an Homocysteinstoffwechsel und -methylierung (siehe Abbildung 5) beteiligt und trägt dazu bei, den Homocysteinspiegel unter Kontrolle zu halten. Methyldonoren wie Cholin haben durch die Methylierung von DNA und Histonen Einfluss auf die Genexpression (aufgrund der Methylierung ist die Transkription eines Gens nicht möglich). Darüber hinaus ist Cholin Precursor des Neurotransmitters Acetylcholin und der Membranphospholipide Phosphatidylcholin und Sphingomyelin. Phosphatidylcholin ist ein Bestandteil von VLDL-Cholesterol und am Fettstoffwechsel und an der Ausscheidung von Fetten aus der Leber beteiligt; das aus Cholin gebildete Betain ist unter anderem für die Nierenfunktion (Reabsorption von Wasser) wichtig. Während der prä- und neonatalen Entwicklung ist für eine gute Ausformung und Reifung des Gehirns und Nervensystems ausreichend Cholin erforderlich.(43) Ein Cholinmangel während der Schwangerschaft erhöht das Risiko für Neuralrohrdefekte, Lippen-Kiefer-Gaumen-Spalten und angeborene Herzfehler. Leberverfettung, Muskelabbau, Angststörungen, beschleunigte Atherosklerose, Hyperhomocysteinämie und die Verschlechterung kognitiver Fähigkeiten können (teilweise) die Folge eines Cholinmangels sein.(43,44) In der Nahrung findet sich Cholin unter anderem in Eiern, Rindfleisch, Huhn, Fisch, Milch, Blumenkohl, Quinoa, Bohnen und Erdnüssen. Die adäquate tägliche Einnahmemenge (Adequate Intake, AI) von Cholin beträgt für erwachsene Frauen 425 mg/Tag (in der Schwangerschaft 450 mg/Tag; in der Stillzeit 550 mg/Tag) und für Männer 550 mg/Tag (Institute of Medicine, United States National Academies).(42). Die unbedenkliche Obergrenze (UL, Upper Limit) für die Einnahme von Cholin beträgt 3500 mg/Tag.Inositol und PABA
Inositol und PABA (para-Aminobenzoesäure) sind streng genommen keine B-Vitamine, dennoch aber oft in Vitamin-B-Komplexen enthalten. In der Natur kommt Inositol am häufigsten in Form von myo-Inositol (Cyclohexan-cis-1,2,3,5-trans-4,6-hexol) vor. Inositol ist unter anderem für den Fettsäurestoffwechsel, die Gallensaftbildung, Hirnfunktion und Insulinwirkung wichtig. PABA, eine Aminosäure, die nicht in Proteine eingebaut wird, schützt vor UV-Strahlung und hilft möglicherweise gegen das Ergrauen der Haare und Haarausfall.
Erläuterung der Begriffe
ACP (Acyl Carrier Proteins): Proteine, die unter anderem an der Synthese von Fettsäuren beteiligt sind
Biotinidase-Mangel: erblich bedingte Stoffwechselkrankheit, bei der Biotin aufgrund eines Mangels an dem Enzym Biotinidase nicht recycelt werden kann, was zu einem schweren Biotinmangel führt
CC-Genotyp (Wild-type) für MTHFR: normales Gen auf beiden Chromosomen eines Chromosomenpaars
CT-Genotyp für MTHFR: ein normales Gen auf dem einen Chromosom und ein verändertes Gen auf dem anderen Chromosom
Cytochrom P450: eine Gruppe von Enzymen, die organische Stoffe oxidiert. Die meisten dieser Enzyme sind wichtig für den Abbau potenziell schädlicher Stoffe und/oder verschiedener körperfremder (xenobiotischer) Stoffe wie z. B. Arzneimittel und Toxine.
Cytosin: heterozyklische organische Base, Baustein von Nukleotiden
Glutathion-Reduktase: Enzym, das ein wichtiges zelluläres Antioxidans (Glutathion) wiederherstellt, nachdem es oxidiert wurde
Heterozygot: zwei verschiedene Ausprägungen eines Gens in einem Chromosomenpaar
Homozygot: zwei identische Ausprägungen eines Gens in einem Chromosomenpaar (das eine Gen stammt vom Vater, das andere von der Mutter)
Megaloblastäre Anämie: makrozytäre Anämie (Blutarmut, gekennzeichnet durch abnorm große rote Blutkörperchen), die durch einen Folat- und/oder Vitamin-B12-Mangel ausgelöst wird
Myoglobin: Sauerstoff bindendes Protein im Muskelgewebe
Nukleotid: allgemeine Bezeichnung für die phosphorsauren Ester der Nukleoside, die aus einem Zucker, einem Phosphat und einer der vier heterozyklischen Basen Adenin, Thymin, Guanin und Cytosin zusammengesetzt sind. Nukleotide sind die Bausteine der DNA (Desoxyribonukleinsäure) und RNA (Ribonukleinsäure).
Panzytopenie: abnormal geringe Anzahl aller (= pan-) Arten von Blutzellen (Leukozyten, Erythrozyten, Thrombozyten)
Polymorphismus: Vielgestaltigkeit, das Auftreten in mehreren Erscheinungsformen/Varianten
Porphyrine: große organische Moleküle mit vier Pyrrol-Einheiten (einer heterozyklischen Verbindung mit der Formel C4H4NH), dazu gehört das Häm (Bestandteil u. a. von Hämoglobin und Myoglobin)
Seborrhoisches Ekzem: eine milde Ekzemform, die Juckreiz, Rötung und Schuppungen im Gesicht entstehen lässt, insbesondere an den Augenbrauen und in den Nasenfalten.
Thymin: heterozyklische organische Base, Baustein von Nukleotiden
TT-Genotyp für MTHFR: verändertes Gen auf beiden Chromosomen
Literaturverweise
1. Thompson JL et al. The science of nutrition, second edition, 2011.2. Blom HJ et al. Overview of homocysteine and folate metabolism. With special references to cardiovascular disease and neural tube defects. J Inherit Metab Dis. 2011;34(1):75- 81.
3. Prinz-Langenohl R et al. [6S]-5-methyltetrahydrofolate increases plasma folate more effectively than folic acid in women with the homozygous or wild-type 677C–>T polymorphism of methylenetetrahydrofolate reductase. Br J Pharmacol. 2009;158(8):2014- 21.
4. Wilcken B et al. Geographical and ethnic variation of the 677C>T allele of 5,10 methylenetetrahydrofolate reductase (MTHFR): findings from over 7000 newborns from 16 areas world wide. J Med Genet. 2003;40(8):619-25.
5. Ueland PM et al. MTHFR polymorphisms and disease. Landes Bioscience 2005.
6. Selhub J. The many facets of hyperhomocysteinemia: studies from the Framingham cohorts. J Nutr. 2006;136(6 Suppl):1726S- 1730S.
7. Wang ZG et al. Association of dietary intake of folate and MTHFR genotype with breast cancer risk. Genet Mol Res. 2014;13(3):5446-51.
8. Yang YM et al. The association between the C677T polymorphism in MTHFR gene and the risk of thyroid cancer: a metaanalysis. Eur Rev Med Pharmacol Sci. 2014;18(15):2097-101.
9. Mei Q et al. The association between MTHFR 677C-T polymorphism and cervical cancer: evidence from a meta-analysis. BMC Cancer. 2012;12:467.
10. Aly RM et al. MTHFR A1298C and C677T gene polymorphisms and susceptibility to chronic myeloid leukemia in Egypt. Int J Clin Exp Pathol. 2014;7(5):2571-8.
11. Victorino DB et al. Meta-analysis of Methylenetetrahydrofolate reductase maternal gene in Down syndrome: increased susceptibility in women carriers of the MTHFR 677T allele. Mol Biol Rep. 2014;41(8):5491-504.
12. Chen JX et al. Genetic polymorphisms in the methylenetetrahydrofolate reductase gene (MTHFR) and risk of vitiligo in Han Chinese populations: a genotypephenotype correlation study. Br J Dermatol. 2014;170(5):1092-9.
13. Cao H et al. Hyperhomocysteinaemia, low folate concentrations and MTHFR C677T mutation in abdominal aortic aneurysm. Vasa. 2014;43(3):181-8.
14. Cao H et al. Homocysteine level and risk of abdominal aortic aneurysm: a metaanalysis. PLoS One. 2014;9(1):e85831.
15. D’Elia PQ et al. MTHFR polymorphisms C677T and A1298C and associations with IVF outcomes in Brazilian women. Reprod Biomed Online. 2014;28(6):733-8.
16. Li SS et al. Prospective study of MTHFR genetic polymorphisms as a possible etiology of male infertility. Genet Mol Res. 2014;13(AOP).
17. Rozycka A et al. Homocysteine Level and Mechanisms of Injury in Parkinson’s Disease as Related to MTHFR, MTR, and MTHFD1 Genes Polymorphisms and L-Dopa Treatment. Curr Genomics. 2013;14(8):534-42.
18. Settin A et al. Association of ACE and MTHFR genetic polymorphisms with type 2 diabetes mellitus: Susceptibility and complications. J Renin Angiotensin Aldosterone Syst. 2014 Jan 22.
19. Pu D et al. Association between MTHFR gene polymorphisms and the risk of autism spectrum disorders: a meta-analysis. Autism Res. 2013;6(5):384-92.
20. Yigit S et al. Association of MTHFR gene C677T mutation with diabetic peripheral neuropathy and diabetic retinopathy. Mol Vis. 2013;19:1626-30.
21. Kalkan G et al. Association of MTHFR gene C677T mutation with recurrent aphthous stomatitis and number of oral ulcers. Clin Oral Investig. 2014;18(2):437-41.
22. Lamers Y et al. Red blood cell folate concentrations increase more after supplementation with [6S]-5-methyltetrahydrofolate than with folic acid in women of childbearing age. Am J Clin Nutr. 2006;84(1):156-61.
23. Bailey RL et al. Serum unmetabolized folic acid in a nationally representative sample of adults ?60 years in the United States, 2001-2002. Food Nutr Res. 2012;56.
24. Bailey RL et al. Unmetabolized serum folic acid and its relation to folic acid intake from diet and supplements in a nationally representative sample of adults aged > or =60 y in the United States. Am J Clin Nutr. 2010;92(2):383-9.
25. Morris MS et al. Circulating unmetabolized folic acid and 5-methyltetrahydrofolate in relation to anemia, macrocytosis, and cognitive test performance in American seniors. Am J Clin Nutr. 2010;91(6):1733-44.
26. Vollset SE et al. B-Vitamin Treatment Trialists’ Collaboration. Effects of folic acid supplementation on overall and site-specific cancer incidence during the randomised trials: meta-analyses of data on 50,000 individuals. Lancet. 2013;381(9871):1029-36.
27. Gezondheidsraad. Naar een optimaal gebruik van foliumzuur. Den Haag: Gezondheidsraad, 2008; publicatienr. 2008/02.
28. EFSA ANS Panel (EFSA Panel on Food Additives and Nutrient Sources added to Food). Scientific
Opinion on (6S)-5-methyltetrahydrofolic acid, glucosamine salt, as a source of folate added for nutritional purposes to food supplements. EFSA Journal 2013;11(10):3358.
29. Horigan G et al. Riboflavin lowers blood pressure in cardiovascular disease patients homozygous for the 677C>T polymorphism in MTHFR. J Hypertension 2010;28:478- 486.
30. Doets EL et al. Systematic review on daily vitamin B12 losses and bioavailability for deriving recommendations on vitamin B12 intake with the factorial approach. Ann Nutr Metab 2013;62:311– 322.
31. Spinneker A, Sola R, Lemmen V et al. Vitamin B6 status, deficiency and its consequences-an overview. Nutr Hosp. 2007;22(1):7-24.
32. Vitamin B6 (pyridoxine and pyridoxal 5’-phosphate) – monograph. Altern Med Rev. 2001;6(1):87-92.
33. Katan MB. Hoeveel vitamine B6 is toxisch? Ned Tijdschr Geneeskd. 2005;149(46):2545-6.
34. Rathanaswami P et al. Effects of thiamin deficiency on the secretion of insulin and the metabolism of glucose in isolated rat pancreatic islets. Biochem Int 1991;25(3):577- 583.
35. Anetor JI et al. Decreased thiamine and magnesium levels in the potentiation of the neurotoxicity of lead in occupational lead exposure. Biol Trace Elem Res. 2007;116(1):43-51.
36. Reddy SY et al. Thiamine reduces tissue lead levels in rats: mechanism of interaction. Biometals. 2010;23(2):247-53.
37. EFSA NDA Panel (EFSA Panel on Dietetic Products, Nutrition and Allergies), 2014. Scientific Opinion on Dietary Reference Values for niacin. EFSA Journal 2014;12(7):3759.
38. Kelly GS. Pantothenic acid. Monograph. Altern Med Rev. 2011;16(3):263-74.
39. Mock DM et al. Marginal biotin deficiency during normal pregnancy. Am J Clin Nutr 2002;75:295-299.
40. Zempleni J et al. Biotin. Adv Nutr. 2012;3(2):213-4.
41. Zempleni J et al. Biotin requirements for DNA damage prevention. Mutat Res. 2012;733(1-2):58-60.
42. Institute of Medicine, and National Academy of Sciences USA. Choline. In: Dietary reference intakes for folate, thiamin, riboflavin, niacin, vitamin B12, panthothenic acid, biotin, and choline. Vol. 1. Washington, D.C.: National Academy Press, 1998:390-422.
43. Zeisel, SH. Choline: Critical role during fetal development and dietary requirements in adults. Annu Rev Nutr 2006;26:229-250.
44. Bjelland et al. Choline in anxiety and depression: the Hordaland Health Study. Am J Clin Nutr 2009;90:1056-60.
45. Scientific Opinion of the Panel on Food Additives, Flavourings, Processing Aids and Materials in Contact with Foods (AFC) on a request from the Commission on Pyridoxal- 5’-phosphate as a source for vitamin B6 added for nutritional purposes in food supplements. The EFSA Journal 2008;760:1- 13.
46. http://books.nap.edu/openbook. php?record_id=6015&page=150
47. Kelly GK. The coenzyme forms of vitamin B12: towards an understandig of their therapeutic potential. Altern Med Rev. 1998;3(1):459-471.
48. Lewis PJ. Pain in the hand and wrist. Pyridoxine supplements may help patients with carpal tunnel syndrome. BMJ. 1995;310(6993):1534.
49. Whyte MP et al. Markedly increased circulating pyridoxal-5’-phosphate levels in hypophosphatasia. Alkaline phosphatase acts in vitamin B6 metabolism. J Clin Invest. 1985;76(2):752-6.
50. Allman MA et al. Elevated plasma vitamers of vitamin B6 in patients with chronic renal failure on regular haemodialysis. Eur J Clin Nutr. 1992;46(9):679-83.
51. Henderson JM et al. The fasting B6 vitamer profile and response to a pyridoxine load in normal and cirrhotic subjects. Hepatology. 1986;6(3):464-71.
52. Levine S et al. Pyridoxine (vitamin B6) neurotoxicity: enhancement by protein-deficient diet. J Appl Toxicol. 2004;24(6):497- 500.
53. Unpublished preclinical study. Intellectual property of Gnosis S.p.A., Italy. www.quatrefolic.com.


Comments are closed.